Caractérisation par la masse volumique
Chaque espèce chimique possède sa propre masse volumique (masse par unité de volume). On la calcule en divisant la masse de l'objet étudié par son volume, son symbole est la lettre grecque ρ (rhô) (parfois la lettre µ (mu) est utilisée)
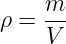
avec : ρ = masse volumique
m = masse de l'objet
V = volume de l'objet
En comparant la masse volumique d'un objet avec des tables qui regroupent des masses volumiques connues, on peut identifier l'espèce chimique qui constitue l'objet.
| En vidéo (par Alloprof) | Exercice (par Paul Olivier, professeur) |
Masses volumiques de quelques métaux :
| Métal | ρ (en g/cm3) |
| aluminium | 2,7 |
| zinc | 7,1 |
| fer | 7,9 |
| cuivre | 8,9 |
| argent | 10,5 |
| plomb | 11,3 |
| or | 19,3 |
Comparaison de la masse volumique de solvants incolores (www.pccl.fr)
Remarques
- Cette méthode fonctionne bien lorsque l'échantillon de matière étudié est "pure". Lorsque plusieurs espèces chimiques sont mélangées, c'est plus compliqué...
- La masse volumique de l'eau est de 1 kg/L (ou 1 g/mL ou encore 1 g/cm3). Tout matériau de masse volumique inférieure à celle de l'eau flotte (huile, bois, plupart des plastiques...), tout matériaux dont la masse volumique est supérieure à celle de l'eau coule (métaux, minéraux...).
Caractérisation par la température de changement d'état
Chaque espèce chimique a ses propres températures de changement d'état. Par exemple, l'eau passe de solide à liquide à une température de 0° Celsius alors que la température de fusion du cyclohexane est à 6,5°C et que celle de l'éthanol est à -114° C.
Ce n'est pas un hazard si la température de fusion de l'eau est de zéro degré Celsius car c'est justement le repère qu'a choisi le physicien suédois Anders Celsius au XXVIIIè siècle comme origine de son échelle. Il plaça ensuite 100° C au niveau de la température d'ébullition de l'eau et gradua régulièrement son échelle.
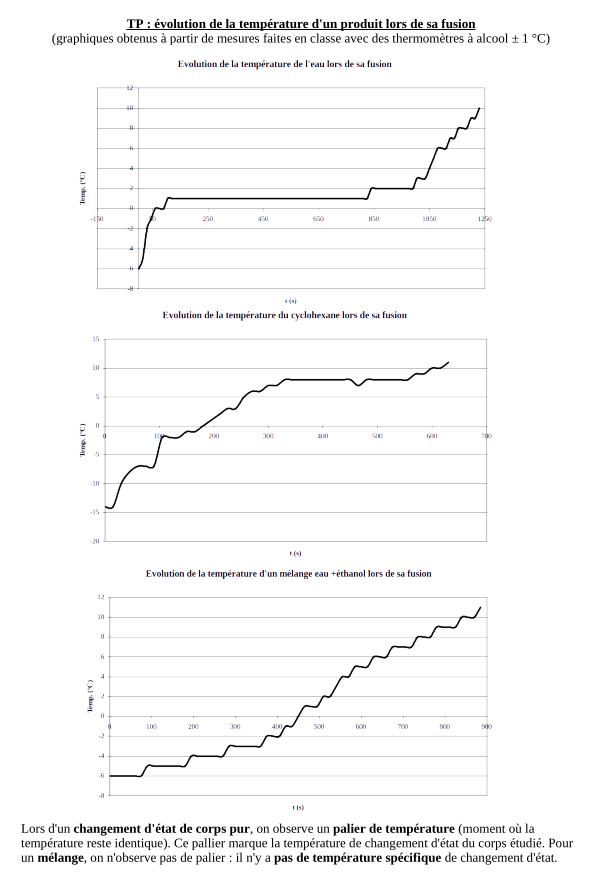
Si l'échantillon étudié est "pur", la température restera la même pendant tout le changement d'état. On observe alors un pallier de température lorsqu'on trace un graphique représentant l'évolution la température en fonction du temps.
Si l'échantillon est un mélange, le changement de température ralentira pendant le changement d'état mais ne stagnera pas.
Point de fusion de quelques métaux
| Aluminium | 660 °C | |
| Argent | 962 °C | |
| Cuivre | 1 085 °C | |
| Étain (blanc) | 232 °C | Utilisé pour les soudures |
| Fer | 1 538 °C | |
| Or | 1 064 °C | |
| Tungstène | 3 422 °C | Filaments des lampes à incandescence |
| Zinc | 420 °C |
Comme pour l'utilisation de la masse volumique, cette méthode fonctionne bien avec des matériaux "purs", pour les alliages c'est plus compliqué...
